Een opa en oma, het lijkt vanzelfsprekend, maar dat is het niet. De mens is een van de weinige soorten waarbij de vrouwen doorleven tot ver na de menopauze. Dat komt waarschijnlijk omdat oma’s nodig waren om de kinderen groot te brengen. Maar wat heeft geslachtsziekte gonorroe daarmee te maken?
Mensenkinderen hebben relatief veel zorg nodig, waar grootmoeder dus fijn een handje bij kan helpen. Dat was heel lang geleden zeker zo, maar geldt stiekem nog steeds: we zijn maar wat blij als oma af en toe bijspringt. Je kunt evolutionair echter wel bedénken dat het handig is als vrouwen ouder worden, er moet ook nog een mechanisme zijn waardoor dat gebeurt. En juist daar hebben onderzoekers van de University of California onderzoek naar gedaan.
Genetische mutaties
Meer precies: ze hebben een aantal genetische mutaties gevonden die ouderen beschermen tegen cognitieve achteruitgang en dementie. In een nieuwe studie, die in Molecular Biology and Evolution verscheen, focussen zij op een van deze gemuteerde genen om zijn evolutiespoor te achterhalen: wanneer en waarom verscheen deze mutatie in het menselijk genoom? De bevindingen wijzen uit dat de selectiedruk (het genetische voordeel voor reproductie) van besmettelijke ziekten, zoals gonorroe ertoe heeft geleid dat deze genvariant in de mens ontstond. Zo bleven mensen langer leven en kregen we dus in tegenstelling tot de meeste andere soorten grootouders.
Het genoom van de meeste diersoorten is geoptimaliseerd voor reproductie, vaak ten koste van de eigen gezondheid en levensverwachting. Doorleven na de menopauze is dan helemaal niet zo vanzelfsprekend, maar het gebeurt wel. Volgens de ‘grootmoederhypothese’ komt dit dus doordat oudere vrouwen een belangrijke rol spelen in de opvoeding van jonge kinderen, die veel meer zorg nodig hebben dan de jongen van andere soorten: de meeste jonge dieren kunnen in no time zichzelf redden.
Chimpansees
Wetenschappers proberen nu te achterhalen welke genetische kenmerken deze hoge levensverwachting mogelijk maken. Toen ze eerder het genoom van een mens en een chimpansee vergeleken, ontdekten ze dat mensen een unieke versie hebben van het gen voor CD33, een receptor in immuuncellen. “De mutatie is een ongebruikelijke variant, die alleen bij mensen voorkomt. Het doel van de evolutie is reproductie. Daar moet deze mutatie een rol in spelen. Mogelijk doordat grootmoeders zo langer leven, die zoals gezegd kunnen helpen met de baby”, vertelt hoofdonderzoeker Ajit Varki, geneeskundeprofessor aan de UC San Diego School of Medicine, in gesprek met Scientias.nl.
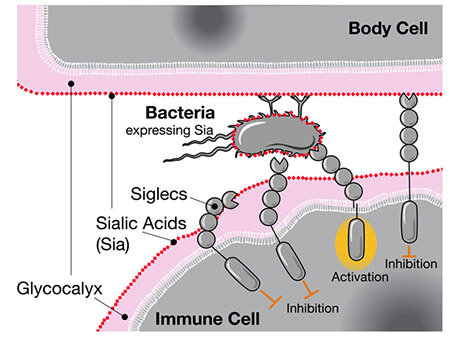
De standaard CD33-receptor bindt zich aan een type suiker dat siaalzuur heet en waarmee alle menselijke cellen bedekt zijn. Als de immuuncel het siaalzuur opmerkt via CD33 herkent het de andere cel als deel van het lichaam en zal hij niet aanvallen. Zo wordt een auto-immuunreactie voorkomen.
Alzheimer
De CD33-receptor is ook terug te vinden in immuuncellen in de hersenen, microgliacellen genaamd. Daar helpt de receptor om neuro-ontstekingen te voorkomen. De microgliacellen spelen een belangrijke rol bij het opruimen van beschadigde hersencellen en amyloïde plaques (de opeenhoping van eiwitfragmenten) die in verband worden gebracht met de ziekte van Alzheimer. Door zich te binden aan de siaalzuren op deze cellen en plaques, onderdrukken de CD33-receptoren echter deze belangrijke microgliale functie en vergroten ze dus het risico op dementie.
Maar daarom is er een nieuwe genvariant ontstaan. Ergens tijdens de evolutie pikten mensen een gemuteerde vorm op van CD33, die zich niet aan de suikers bindt. De gemuteerde receptor reageert niet langer met de siaalzuren van beschadigde cellen en plaques, waardoor de microglia de kans krijgen om ze af te breken. Hogere niveaus van deze CD33-variant bleken juist te beschermen tegen alzheimer.
Natuurlijke selectie
Tijdens de zoektocht naar een verklaring voor het ontstaan van deze genvariant vonden Varki en zijn collega’s bewijs voor een sterke positieve selectie, suggererend dat er iets was dat het gen dreef om sneller te evolueren dan verwacht. Ze ontdekten ook dat deze specifieke versie van CD33 niet aanwezig was in het genoom van Neanderthalers of Denisovans, evolutionair gezien onze nauwste verwanten.
“Bij de meeste genen die verschillend zijn tussen mensen en chimpansees hebben Neanderthalers dezelfde versie als mensen, dus het was verrassend dat dit nu niet zo was”, aldus Varki. “Deze bevindingen suggereren dat de wijsheid en zorg van gezonde grootouders een belangrijk evolutionair voordeel was dat wij wel bezaten en andere mensensoorten niet. Het draagt er mogelijk aan bij dat wij overleefden en de Neanderthalers bijvoorbeeld uitstierven.”
Nieuw bewijs grootmoederhypothese
Volgens de onderzoekers levert hun studie nieuw bewijs voor de grootmoederhypothese. Maar toch: de evolutietheorie schrijft voor dat voortplanting de belangrijkste drijfveer is voor genetische selectie en niet cognitieve gezondheid na de vruchtbare levensfase. Dus wat zorgde ervoor dat deze gemuteerde vorm van CD33 bij mensen toch naar bovenkwam?
Een mogelijkheid is dat besmettelijke ziektes, zoals gonorroe, een negatieve invloed hadden op de vruchtbaarheid en zo impact hadden op de menselijke evolutie. Gonorroe-bacteriën bedekken zich met dezelfde suikers als de CD33-receptoren. Dus als een wolf in schaapskleren zijn de bacteriën in staat om de menselijke immuuncellen te laten geloven dat ze geen gevaarlijke indringers zijn van buiten. Terwijl ze dat natuurlijk wel zijn.
De onderzoekers denken dat de gemuteerde versie van CD33 ontstond als de menselijke aanpassing tegen zulke ‘moleculaire nabootsing’ van gonorroe en andere pathogenen. Ze konden bevestigen dat een van de mens-specifieke mutaties in staat was om de interactie tussen de bacteriën en CD33 compleet te vernietigen, waardoor immuuncellen opnieuw de bacteriën konden aanvallen.
In eerste en in tweede instantie
De onderzoekers zijn ervan overtuigd dat mensen in eerste instantie de gemuteerde vorm van CD33 geërfd hadden om in de vruchtbare jaren beschermd te zijn tegen gonorroe. Later is deze genvariant overgenomen door de hersenen vanwege zijn voordelen als het gaat om de bescherming tegen dementie. “Het is heel goed mogelijk dat CD33 een van de vele genen is die is geselecteerd vanwege zijn voordeel in de strijd tegen infectieziekten vroeg in het leven, maar dan in tweede instantie is geselecteerd vanwege het beschermende effect tegen dementie en andere leeftijdsgerelateerde ziektes”, aldus antropologie- en pathologieprofessor Pascal Gagneux, die het onderzoek samen met Varki leidde.
Zo speelt gonorroe compleet toevallig een belangrijke rol in de evolutie van de mens. “Het is een denkfout dat de evolutie helemaal logisch is”, legt Varki uit. “Het gebeurt gewoon toevallig. Je hebt de neiging om te denken dat het allemaal een bedoeling heeft, maar dat is niet zo. Het is compleet willekeurig.”
Omstreden
De grootmoederhypothese is niet onomstreden, geeft Varki toe. Er zijn ook studies die de evolutionaire verklaring weerspreken, onder meer omdat de rol van grootvaders onduidelijk is. “Een hulpeloze baby heeft een grootmoeder nodig dus dat vrouwen na de menopauze blijven leven is te verklaren, maar grootvaders zijn veel minder nuttig. Het lijkt er op dat de opa’s mee konden liften op de voortlevende oma’s, maar dat is speculatie”, aldus Varki.
Hij vindt het bijzonder dat gonorroe eerst een gevaar was en later voor een evolutionair voordeel zorgde. “In eerste instantie verkleinde gonorroe juist de kans op reproductie. Dus het moest worden gecanceld, maar toen bleek de genmutatie erg nuttig voor de hersenen en bleef hij bestaan.” Het maakt ook duidelijk hoe willekeurig de evolutie verliep en dat het puur toeval is dat wij mensen zijn zoals we zijn.





